生物材料植入后与机体的相互作用关系主要发生于材料表面界面。众多研究表明,材料表面界面的物理或化学性质是影响细胞行为和组织再生的关键因素。
因此,体外或体内研究生物材料的表面界面性质与细胞、组织的相互作用关系及分子机制,对医用高分子的设计与改性,改善材料的生物相容性和生物活性,提高材料的组织再生能力具有重要的研究与应用价值。具体方法是:
首先,我们通过建立相应的材料学和生物学研究方法,从分子、亚细胞、细胞和整体等不同水平研究不同表面界面性质的材料对细胞行为和功能的影响,评估材料的生物相容性和生物活性,探索其相互作用的分子机制,为新材料的设计、改性及其在组织工程和再生医学中的应用提供科学依据;
其次,通过物理或化学手段将特定功能的生物分子固定于材料表面,研究胚胎或成体干细胞的分化诱导因素和机制,仿生构筑有利于干细胞生存和发育的微环境,探索干细胞安全、有效地应用于体内的新材料技术;
同时,通过施加电/磁信号、光信号和力学刺激,研究材料表面细胞的生物学效应和机制,开发材料植入体内后的物理治疗手段,以增强材料的组织再生修复能力。
  |
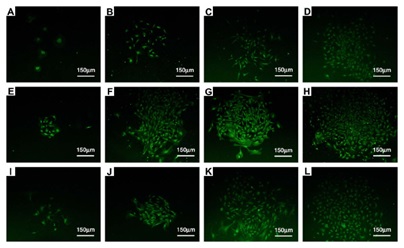 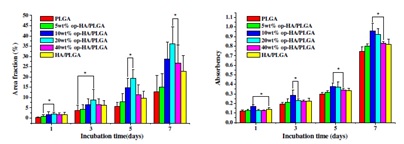 |
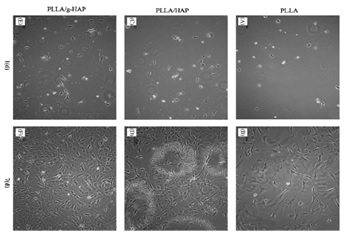
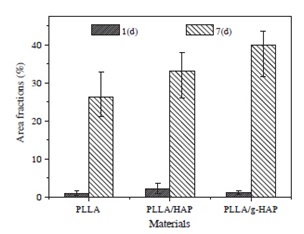
Human condrocytes /rabbit osteoblasts grew on the surfaces of g-HAP/PLGA nanocomposites(Biomaterials, 2005,26, 6296-304; Acta Biomaterialia 2009;5:2680-9)
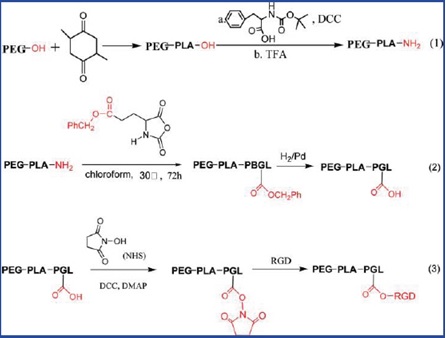  |
RGD conjugates for cell adhesion and bone tissue engineering
(Biomacromolecules 2011; 12 (7): 2667-80 )
|
|
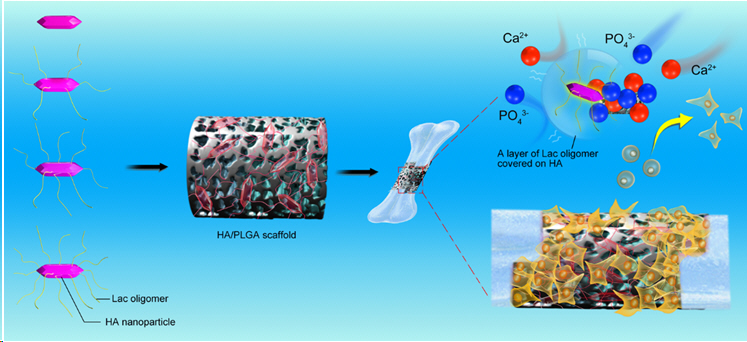
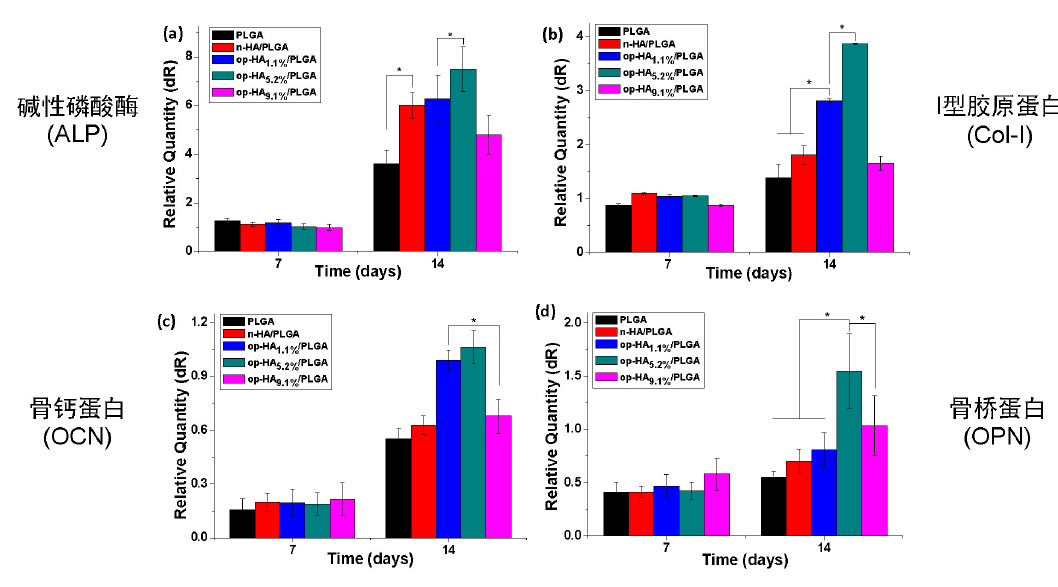
Enhanced osteogenic genes expression of composite scaffolds through controlled surface grafting
of L-lactic acid oligomer on nano-hydroxyapatite.
(Biomacromolecules, 2016, 17 (3):818–829)
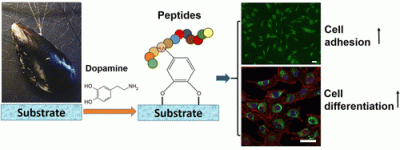
Poly(dopamine)-assisted immobilization of collagen mimetic peptide (CMP) and osteogenic growth peptide (OGP) on the surface of op-HA/PLGA nano-composite for improving cell adhesion and osteogenesis.
(ACS Appl Mater Interfaces. 2016 Oct 12;8(40):26559-26569)
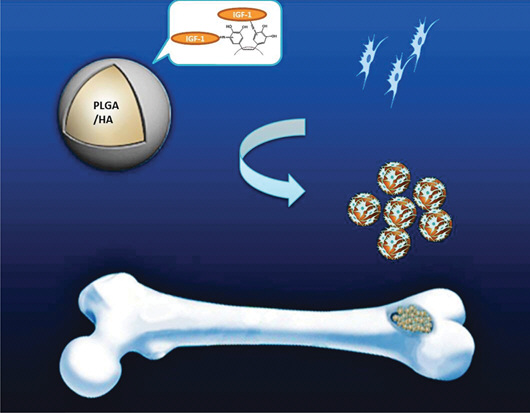 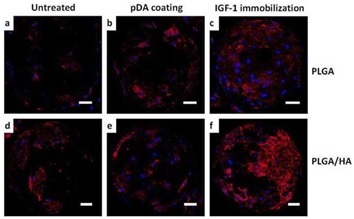 |
Immobilization of IGF-1 on biodegradable microcarriers of HA/PLGA for bone tissue engineering
(Macromol Biosci. 2015,15(8):1070-80).