人类多能干细胞(hPSC)作为成人细胞的来源,在治疗从糖尿病到肝功能衰竭等疾病方面具有很大的前景。限制hPSCs临床/转化影响的一些挑战是现有分化方案的高成本和难以扩展。
人类多能干细胞(hPSC)无限期增殖,并可分化为任何成体细胞类型。这使hPSCs成为再生医学和组织工程应用的优秀细胞源。hPSC的维持和分化方案依赖于诱导线索,通常是生长因子(GFs),在几天和几周的过程中,每天以纳克/毫升的量添加到培养基中。虽然这种分化方案已经建立并具有特征,但需要大量的重组GFs,这使得扩大到更大体积的干细胞培养成本高昂。 肝素是一种天然多糖和ECM成分,已用于设计能够隔离和释放GFs的生物材料。多年来,含肝素的水凝胶已用于装载和控制释放多种GFs,包括酸性和碱性成纤维细胞生长因子(aFGF和bFGF)、肝细胞生长因子(HGF)、血管内皮生长因子(VEGF)、转化生长因子(TGF)-β1和结节。除了装载和释放GFs外,许多研究表明,含肝素的支架有助于改善包埋细胞的增殖、分化和功能。
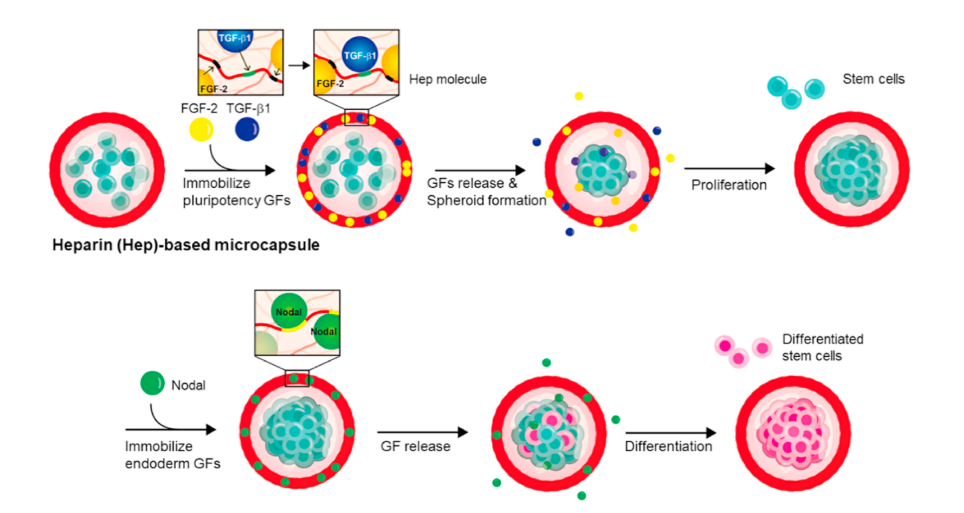
近日,梅奥医学中心的Gwon Kihak等人开发包含肝素部分的水凝胶微胶囊,用于GF负载和用于hESC聚集和球体形成的水核。分析了生物活性微囊的多能性信号FGF-2和TGF-β1的释放曲线,以及内胚层信号Nodal。同时证明还证明,多能性和内胚层信号可以从相同的微囊中顺序加载和释放。与使用可溶性GFs的标准方案相比,一次性加载和持续释放诱导线索使我们能够将维持多能性和内胚层分化所需的GF量减少5倍。除了降低成本外,与标准方案相比,从生物活性微囊局部释放GFs导致hPSCs表达更高水平的多能性和内胚层标记物。
Recently, gwonkihak of Mayo Medical Center and others developed hydrogel microcapsules containing heparin for GF loading and water core for hESC aggregation and sphere formation. The pluripotent signals FGF-2 and TGF of bioactive microcapsules were analyzed- β 1, and endoderm signal nodal. It was also proved that pluripotency and endodermal signals could be loaded and released from the same microcapsules in sequence. Compared with the standard protocol using soluble GFS, one-time loading and continuous release of induced cues enabled us to reduce the amount of GF required to maintain pluripotency and endodermal differentiation by five times. In addition to reducing costs, the local release of GFS from bioactive microcapsules resulted in higher levels of pluripotent and endodermal markers expressed by hpscs compared with the standard protocol.
DOI:10.1016/J.BIOACTMAT.2021.12.008
王天明